-

Introduction
Les dragons barbus (Pogona vitticeps) sont originaires d’Australie et sont des animaux de compagnie populaires. Les éleveurs effectuent souvent une sélection sur le tempérament et les couleurs, de manière à fournir une variété de plus en plus grande sur le marché des reptiles. Les dragons barbus sont également élevés en élevages commerciaux et vendus dans la plupart des animaleries, en faisant des reptiles de compagnie facilement accessibles. Les dragons barbus sont appréciés pour leur tempérament naturellement calme, en plus de leur taille relativement petite et leurs conditions d’entretien et de manipulation peu contraignantes. La population de pogonas de compagnie grandissant, la probabilité de les rencontrer en consultation augmente proportionnellement.
-

Informer les clients
Informer les propriétaires sur les conditions d’entretien de leur animal constitue la base de la médecine préventive de tous les NAC. Avec l’amélioration continue des conditions de vie des NAC via l’information des clients et la création de liens forts entre les propriétaires et leurs reptiles de compagnie, les maladies infectieuses, tumorales et gériatriques vont probablement devenir des motifs de consultation plus fréquents. Cette présentation est conçue comme une référence de base pour les vétérinaires praticiens à propos des principales maladies infectieuses des pogonas.
Please note this content is not intended to be an all-inclusive list and continued visitation of current literature to identify novel and emerging diseases affecting exotic pet species is recommended.
Veuillez noter que cette présentation ne se veut pas exhaustive et qu’il reste recommandé de consulter régulièrement les dernières parutions de la littérature scientifique pour se tenir au courant des nouvelles maladies ou des maladies émergentes des NAC.
Crédit photo : Resa McLellan
-

Oxyures (Oxyuris spp.)
Les oxyures sont communs chez les reptiles en captivités et dans la nature.
Crédit photo : Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-

Oxyures : Maladie clinique
La plupart du temps, les oxyures sont considérés comme des parasites commensaux non pathogènes et sont suspectés d’aider l’hôte à digérer la cellulose dans les matières fécales et ainsi d’éviter la constipation (Telfor and Campbell 1981). Dans de rares cas, une charge parasitaire importante peut être responsable d’une impaction du colon.
Signes cliniques : Il est rare d’observer des signes cliniques lors d’infestation par des oxyures.
Lésions : Bien que les colites (inflammation du colon) ne soient pas typiques des infections par des oxyuryes, les oxyures, compte tenu de leur cycle direct, peuvent dans de rares cas être responsables de charges parasitaires telles qu’elles causent une impaction colique.
Illustré ici, des oxyures adultes dans une portion de colon dilatée.
Crédit photo : Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-

Oxyures : Oeufs
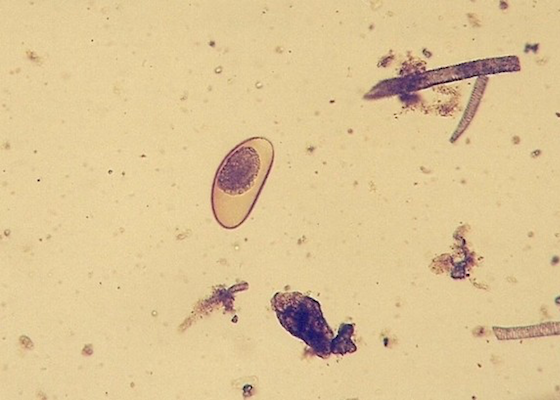
Diagnostic : Le diagnostic se fait par l’identification d’oeufs dans les fèces par frotti direct ou technique de flottation. Les œufs sont de grande taille, environ 130 µm x 40 µm et peuvent être embryonnés (non systématique) (Jacobson 2007).
Illustré ici, un œuf d’oxyure
Crédit photo : Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-
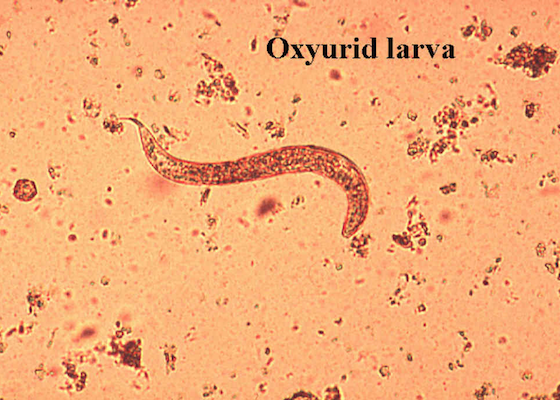
Oxyures : vers adultes
Diagnostic : Parfois des vers adultes peuvent être trouvés dans les fèces.
Illustré ici, une larve d’oxyure
Crédit photo: Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-
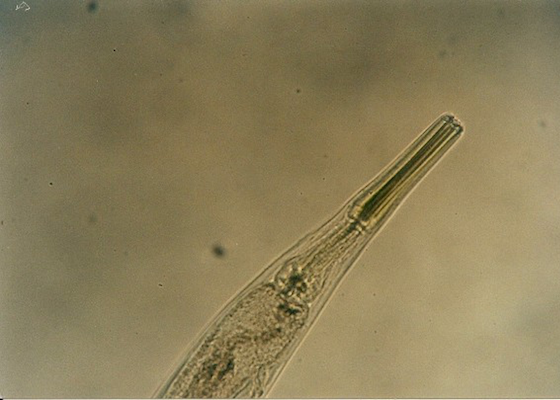
Oxyures
Illustré ici, l’extrémité antérieure d’un oxyure chez un iguane vert (Iguana iguana).
Crédit photo : Rataj AV et al. Les parasites des reptiles de compagnie. Acta Vet Scand 53(1):33, 2011. Utilisé avec la permission de l’auteur.
-
Oxyures : Transmission, Contrôle & Traitement
Transmission & contrôle : Les oxyures sont transmis par voie féco-orale et ont un cycle de vie direct. Après ingestion, les œufs se transforment en larves dans l’intestin proximal avant de migrer jusqu’au rectum sous forme adulte.
Pinworms are highly host specific. Therefore, there is little risk of transmission between bearded dragons and other pets in the household, including other reptiles. Reptile pinworms are not known to be transmissible to humans. Control is by quarantine of new individuals, routine fecal examinations, and treatment of infected individuals prior to introduction into a collection.
Les oxyures sont très spécifiques d’espèce. Ainsi, il y a très peu de risque de transmission entre les dragons barbus et les autres animaux de compagnie, notamment les autres reptiles. Les oxyures des reptiles ne sont théoriquement pas transmissibles aux humains. La prévention passe principalement par la quarantaine des nouveaux individus, la réalisation d’analyses de selles (coproscopies) régulières, et le traitement des individus infectés avant leur introduction dans une collection.
Traitement : Fenbendazole 50 mg/kg PO (Lane and Mader 1996) Imidacloprid et moxidectine (Advantage multi/Advocate, Bayer, Shawnee, Mission, KS), par voie topique (Groza et al 2009)
Illustré ici, un oeuf d’oxyure (espèce non identifiée) chez un iguane vert (Iguana iguana).
Crédit photo : Rataj AV et al. Parasites des reptiles de compagnie. Acta Vet Scand 53(1):33, 2011. Utilisé avec la permission de l’auteur.
-

Nannizziopsis spp.
Le complexe Chrysosporium anamorph of Nannizziopsis vriesii (CANV) (Maladie du « champignon jaune » ou Yellow Fungus Disease)
La taxonomie du complexe Chrysospsorium anamorph of Nannizziopsis vriesii (CANV) a récemment été réévaluée basée sur le séquençage moléculaire, le séparant ainsi en 3 genres : Nannizziopsis, Paranannizziopsis, et Ophidiomyces (Sigler et al 2013). Les champignons du genre Nannizziopsis sont considérés comme les agents responsables de la maladie du “champignon jaune”, avec N. chlamydospora, N. draconii, N. barbata, N. guarroi, et N. vriesii ayant été isolés chez des dragons barbus atteints de la maladie. Ces champignons sont kératinophiles et peuvent causer des dermatomycoses sévères et souvent fatales. (Bowman et al 2007). Nannizziopsis spp. est rarement isolé de la peau de reptiles sains et est considéré comme un agent pathogène primaire.
Illustré ici, La coloration jaune de la peau, caractéristique de la maladie, sur l’abdomen d’un dragon barbu. Bien que fortement suggestive de la maladie, cette lésion n’est pas spécifique de la « Yellow Fungus Disease » (voir diapositive suivante).
Crédit photo: Nicholas A. Crossland, DVM, DACVP
-

Nannizziopsis: Signes cliniques
Le complexe Chrysosporium anamorph of Nannizziopsis vriesii (CANV) ) (Maladie du « champignon jaune » ou Yellow Fungus Disease)
Signes cliniques : Les lésions peuvent commencer sous forme de décolorations cutanées jaunes localisées ou multifocales, donnant à la maladie ce surnom de “Yellow Fungus disease” ou maladie du “champignon jaune”. Les lésions progressent et deviennent irrégulières multifocales à coalescentes avec épaississement cutané, exsudation et hyperkératose. Moins fréquemment, la dermatite se manifeste sous la forme de nodules cutanés (Reavill and Griffin 2013). Ces zones de peau épaissie ou mes nodules cutanés peuvent devenir ulcératifs.
Lésions : La croissance fongique est initialement limitée à la couche de kératine épidermique superficielle, se manifestant par l’hyperkératose et la décoloration jaune de la peau. Puis la croissance fongique s’étend progressivement au derme sous-jacent, aux muscles squelettiques et parfois aux os, causant une inflammation granulomateuse avec de hyphes intralésionnels.
Illustré ici, Nodules recouvrant la paupière gauche d’un dragon barbu. Histologiquement, ce nodule était composé d’une inflammation granulomateuse autour d’hyphes fongiques. Les nodules peuvent exfolier et devenir ulcérés.
Crédit photo: Nicholas A. Crossland, DVM, DACVP
-

Nannizziopsis: Diagnosis
Diagnostic
Le complexe Chrysosporium anamorph of Nannizziopsis vriesii (CANV) ) (Maladie du « champignon jaune » ou Yellow Fungus Disease)
Les lésions dermatologiques peuvent permettre de suspecter la maladie et le diagnostic antemortem présomptif peut être posé via la réalisation de biopsies des lésions cutanées par des laboratoires expérimentés. L’identification histologique d’hyphes d’apparence typique associée à l’isolation de colonies fongiques blanches-poudrées contenant à la fois des aleuroconidies solitaires et des chaînes d’arthroconidies sont très suggestifs de Nannizziopsis spp., cependant une PCR avec séquençage est nécessaire pour le diagnostic de certitude. Récemment, l’apparence cytologique des lésions de Yellow Fungus Disease a été décrite, apportant aux cliniciens une façon rapide de renforcer la suspicion diagnostique (Le Donne et al 2016).
Note de l’auteur : Des décolorations cutanées jaunes similaires ont été décrites lors d’infections concomitantes par Malessezia sp. et Staphylococcus xylosus chez des dragons barbus, soulignant l’importance des examens complémentaires pour obtenir un diagnostic de certitude.
Illustré ici, Des hyphes de Nannizziopsis guarroi/em> au sein de débris de kératine chez un dragon barbu. Les hyphes sont mis en évidence par la coloration à l’acide périodique de Schiff (PAS).
Crédit photo: Nicholas A. Crossland, DVM, DACVP
-
 Nannizziopsis: Transmission, traitement et contrôle
Nannizziopsis: Transmission, traitement et contrôle
Le complexe Chrysosporium anamorph of Nannizziopsis vriesii (CANV) ) (Maladie du « champignon jaune » ou Yellow Fungus Disease)
-
 Coccidies (Isospora amphiboluri)
Coccidies (Isospora amphiboluri)
Cycle biologique (Lane et Mader 1996): Isospora amphiboluri a un cycle direct passant par une reproduction à la fois asexuée et sexuée au sein du même hôte. Les fèces contiennent des oocystes non sporulés qui sont déposés dans l’environnement. Les hôtes s’infectent via l’ingestion d’oocystes sporulés matures, après maturation dans l’environnement. Les oocytes relarguent des sporocystes, qui à leur tour relarguent des sporozoïtes dans le tube digestif, et colonisent les cellules épithéliales de la muqueuse intestinales dans lesquelles ils maturent en schizontes. Les schizontes matures entraînent la rupture des entérocytes, relarguant ainsi des mérozoïtes qui peuvent directement infecter les autres cellules épithéliales dans lesquelles elles forment à nouveau des schizontes ou se transforment en macro- et microgamétocytes. Ces derniers sont fécondés et forment alors des oocytes, qui sont évacués dans les fèces.
Signes cliniques : Les dragons barbus atteints de coccidiose peuvent présenter de l’anorexie ou de la diarrhée. Dans les cas sévères, les animaux peuvent régurgiter, être déshydratés ou présenter une entérite hémorragique.
strong>Lésions : La réplication de Isospora amphiboluri au sein des cellules épithéliales de l’intestin grêle suivie de la rupture des schizontes est responsable de nécrose, avec possible ulcérations, et de fibrose. Dans les cas sévères, un sepsis peut se développer suite aux ulcérations qui peuvent permettre la translocation de bactéries depuis le tube digestif.
-

Coccidies : diagnostic, traitement et contrôle
Diagnostic : Le diagnostic peut être posé via l’identification d’oocystes lors d’une analyse de selles avec examen microscopique direct ou technique de flottation. Les oocystes de Isospora amphiboluri contiennent deux sporocystes, chacun contenant quatre sporozoïtes. Les oocystes mesurent 23 à 26 µm par 23 à 26 µm (McAllister et al 1995).
Traitement et contrôle : Le traitement actuellement recommandé est le ponazuril 30 mg/kg PO q 48 heures pour 2 traitements (Bogoslavsky 2007). Auparavant, l’utilisation de la sulfadiazine triméthoprime à la dose de 30 mg/kg IM q24h pendant 2 jours, puis 15 mg/kg IM q 48h pour 5 traitements avait été décrite (Lane and Mader 1995).
Le contrôle de la coccidiose passe par la mise en quarantaine des nouveaux individus, la réalisation d’analyses de selles, et le traitement des individus atteints avant leur introduction dans une collection. Il est important de bien insister sur la nécessité d’une bonne hygiène (Gibbons 2014).
Illustré ici, Isospora sp. chez un dragon barbu (P. vitticeps).
Crédit photo : Rataj AV et al. Parasites des reptiles de compagnie. Acta Vet Scand 53(1):33, 2011. Utilisé avec la permission de l’auteur.
-
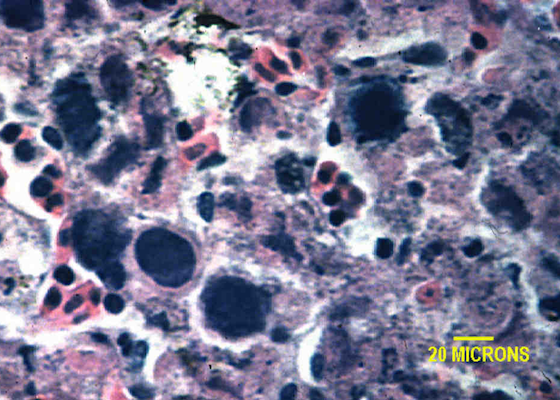
Adénovirus des Agamidés (Agamid AdV1)
L’adénovirus des Agamidés (ou Agamid Adenovirus AdV1) touchant les dragons barbus est un virus enveloppé à ADN double brin, spécifique d’espèce, qui est maintenant endémique aux Etats Unis (Reavill and Griffin 2014, Schumacher 1996). La majorité des cas surviennent chez des jeunes animaux de moins d’un mois et jusqu’à 12 semaines d’âge, mais la maladie a également été décrite chez des individus plus âgés jusqu’à 8 mois (Moormann et al 2009, Doneley et al 2015). Les cas surviennent de manière sporadique ou sous forme d’épidémies au sein de colonies (Reavill and Griffin 2014, Schumacher 1996).
Transmission: La contamination se fait surtout par voie féco-orale. La transmission verticale via les œufs est en cours d’investigation (Reavill and Griffin 2014, Schumacher 1996).
Signes cliniques : Les animaux peuvent être présentés pour de l’anorexie intermittente ou de la léthargie, des retards de croissance ou de l’amaigrissement avec de l’opisthotonos, un torticolis ou des épisodes où ils tournent en rond. Bien que cela soit moins fréquent, des stomatites, pneumonies et parésies postérieures ont aussi été décrites. Les signes cliniques sont souvent plus sévères chez les jeunes animaux, les animaux stressés ou ceux atteints de maladies concomitantes (par exemple, des coccidioses intestinales). Il n’est pas rare d’observer un amaigrissement important, une émaciation et de fort taux de mortalité chez ces individus (Reavill and Griffin 2014, Schumacher 1996).
Lésions : Le foie est typiquement diffusément augmenté de taille et pâle. Histologiquement, des zones de nécrose hépatique multifocales sont associée à la présence de corps d’inclusion intranucléaires basophiliques à amphophiliques dans les hépatocytes (Reavill and Griffin 2014, Schumacher 1996).
There is an incoherence here : inclusions are described as « eosinophilic to amphophilic » in this paragraph, and later described as « basophilic ». According to the references cited here, inclusions appear to be basophilic, so I corrected it in the text.
Illustré ici, Infection d’un jeune Pogona henrylawsoni par l’adénovirus. L’infection chez P. vitticeps est morphologiquement identique.
Crédit photo: Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-

Adénovirus : diagnostic
Le diagnostic ante-mortem est basé sur une PCR sur écouvillon cloacal. Pour un diagnostic post-mortem, la PCR doit être effectuée de préférence sur le foie ou sur un écouvillon intestinal. Le diagnostic peut également être posé via l’histologique qui peut mettre en évidence une nécrose hépatique avec de larges inclusions intranucléaires basophiliques intralésionnelles.
Crédit photo: Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-
Adénovirus des Agamidés : lésions
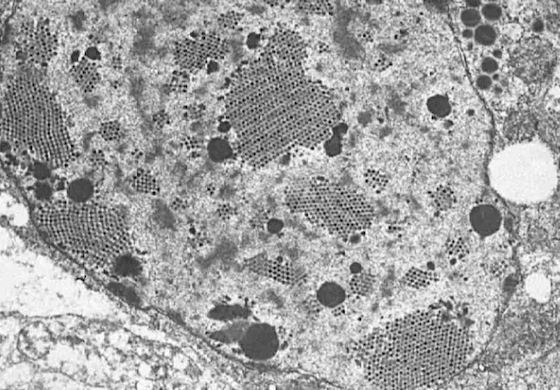
Lésions histologiques : Les corps d’inclusion intranucléaires, qui sont particulièrement visibles dans les hépatocytes, peuvent être observés dans les épithéliums biliaires, rénaux, de l’intestin grêle et du gros intestin, du pancréas et de la muqueuse buccale. La microscopie électronique peut mettre en évidence des particules virales aux nucléocapsides icosaédriques mesurant 80 à 110 nm de diamètre, organisées en réseaux paracristallins (Reavill and Griffin 2014, Moorman et al 2009, Schumacher 1996).
Illustré ici, des réseaux paracristallins adénoviraux au microscope électronique à transmission Pogona henrylawsoni
Crédit photo: Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-
Adénovirus des Agamidés : microscopie électronique
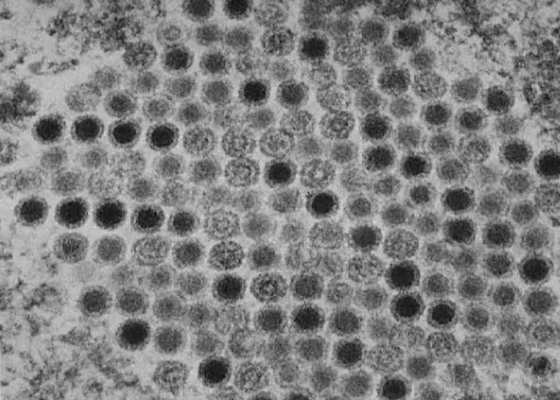
La microscopie électronique peut mettre en évidence des particules virales aux nucléocapsides icosaédriques mesurant 80 à 110 nm de diamètre, organisées en réseaux paracristallins (Reavill and Griffin 2014, Moorman et al 2009, Schumacher 1996).
Illustré ici, des réseaux paracristallins adénoviraux au microscope électronique à transmission Pogona henrylawsoni
Crédit photo: Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-
Adénovirus : traitement & contrôle
Traitement & contrôle : A l’heure actuelle, il n’y a aucun traitement efficace pour les infections adénovirales chez les dragons barbus et aucun vaccin n’est disponible. Les antibiotiques doivent être considérés en cas d’infection bactérienne secondaire et les antiparasitaires pour les infections concomitantes (Reavill and Griffin 2014, Schumacher 1996).
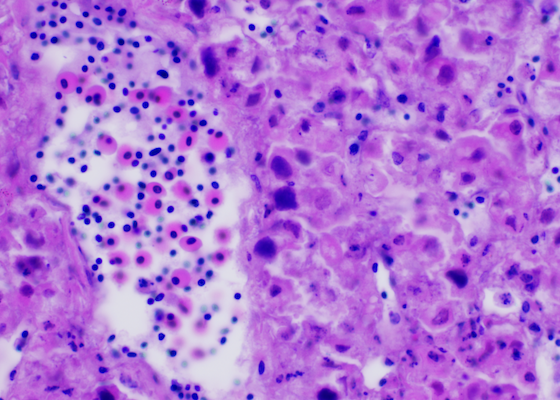
Illustré ici, une infection adénovirale chez un jeune dragon barbu avec des inclusions intranucléaires basophiles bien visibles au sein des hépatocytes.
Crédit photo: Nicholas A. Crossland, DVM, DACVP
-

Cryptosporidium spp.
Cryptosporidium est un parasite protozoaire coccidien.
Transmission : Cryptosporidium se transmet par voie féco-orale ou par des matières contaminées. Les oocystes sporulés sont émis dans les fèces des hôtes infectés, et sont immédiatement infectants. Bien que ce parasite ne soit pas spécifique d’espèce, les cryptosporidies des reptiles ne sont pas connues pour être contagieuses pour les humains. Les proies animales ne sont pas considérées comme des sources de contamination pour les reptiles de compagnie (Lane and Mader 1996, Cranfield and Graczyk 1996).
Signes cliniques : A ce jour, Cryptosporidium n’a pas été associé à des signes cliniques ou des lésions pathologiques chez les dragons barbus. Cryptosporidium est connu pour causer des gastrites prolifératives sévères chez les serpents. Les animaux peuvent devenir sévèrement émaciés et déshydratés, ainsi que présenter de la diarrhée qui peut parfois être hémorragique. L’amaigrissement chronique peut mener au décès de l’animal (Reavill and Griffin 2014, Cranfield and Graczyk 1996). Illustré ici, Cryptosporidium adhérant à la muqueuse, mis en évidence par une coloration de Giemsa.
Crédit photo: Nicholas A. Crossland, DVM, DACVP
-
Cryptosporidium : Signes cliniques
Bien que Cryptosporidium semble être asymptomatique chez les dragons barbus, les animaux porteurs peuvent transmettre le parasite aux espèces sensibles (par exemple, les geckos léopards ou les serpents) dans une collection ou au sein d’une maison (Cranfield and Graczyk 1996). Malgré le traitement, le taux de mortalité approche les 100% chez les animaux sensibles atteints de cryptosporidiose. Les infections concomitantes (par exemple, l’adenovirus) peuvent aggraver les signes cliniques et augmenter le risque de mortalité.
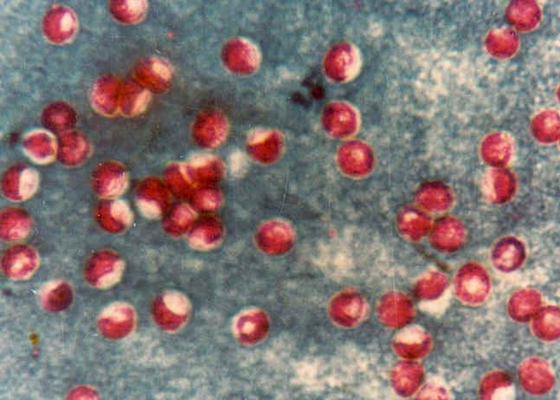
Illustré ici, Cryptosporidium sur une coloration de Ziehl-Neelson.
Crédit photo: Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-
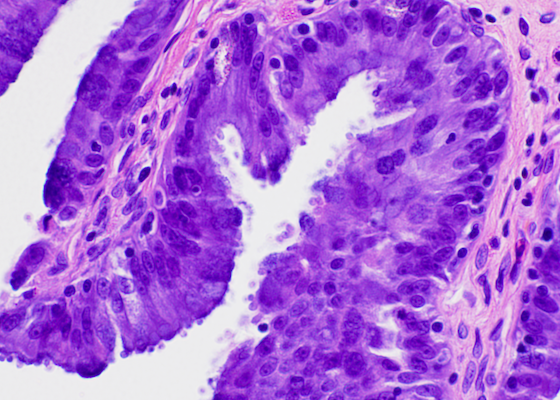
Cryptosporidium spp.: Lésions
Aucune inflammation significative n’est associée à la présente de Cryptosporium, en corrélation avec l’absence de signes cliniques. Les organismes recouvrent souvent la surface apicale des entérocytes, principalement dans le tiers distal du tube digestif. Les organismes sont particulièrement mis en évidence par une coloration de Giemsa. Les organismes sont intracellulaires, mais extracytoplasmiques lorsqu’ils sont observés au microscope électronique.
Illustré ici, des cryptosporidies recouvrant l’épithélium intestinal d’un dragon barbu.
Crédit photo: Nicholas A. Crossland, DVM, DACVP
-
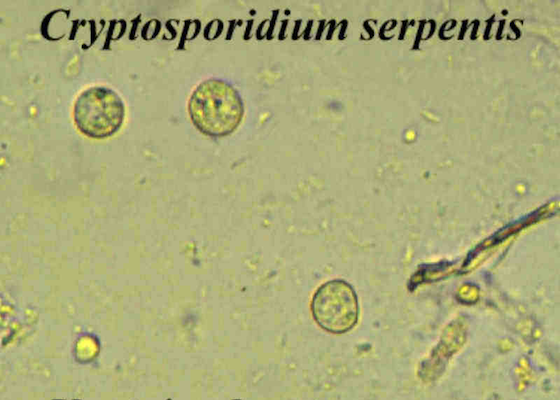
Cryptosporidium : Diagnostic
La cryptosporidiose est diagnostiquée via l’observation d’oocystes sur des frottis de selles colorés. Les oocystes de Cryptosporidium contiennent quatre sporozoïtes sans sporocystes, et font moins de 4 microns de diamètre. Les colorations d’Acide périodique de Schiff (PAS) ou Hématoxyline de Mayer sont recommandées pour faciliter l’identification (Cranfield and Graczyk 1996).
Illustré ici, un examen direct de selles mettant en evidence Cryptosporidium serpentis.
Crédit photo: Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-

Traitement et contrôle
La paromycine est un aminoglycoside très peu absorbé par voie orale. Administrée à 360 mg/kg q 48h pendant 10 jours, elle permet d’éliminer efficacement l’excrétion fécale (Grosset et al 2011). Les oocystes sont résistants et la décontamination de l’environnement nécessite 18 heures de contact avec de l’ammoniac à 5%. Les matières contaminées potentielles doivent aussi être désinfectés avec des solutions d’ammoniac et laissées à l’air libre pour sécher pendant 3 jours avant d’être réutilisées (Cranfield and Graczyk 1996).
Illustré ici, Cryptosporidium avec une coloration au thiomersal.
Crédit photo: Fredric L. Frye, BSc, DVM, MSc, CBiol, FSB, FRSM, Hon DABVP, Hon DECZM
-
Résumé
Ce diaporama sur le dragon barbu résume les maladies infectieuses importantes de ce lézard populaire, incluant la “Yellow Fungus Disease”, l’adénovirus des Agamidés, les oxyures et les cryptosporidies. Le tableau clinique associé à ces infections varie de l’absence de symptômes comme avec les oxyures ou Cryptosporidim, aux lésions dermatologiques associés au complexe Chrysosporium anamorph of Nannizziopsis vriesii (CANV) ou « Yellow Fungus Disease ». Une large gamme de signes cliniques peut être observée avec l’adénovirus des Agamidés, incluant des signes non-spécifiques de maladie, des troubles neurologiques, des stomatites et/ou des pneumonies, particulièrement chez les animaux jeunes ou souffrant d’affections concomitantes.
Crédit photo : Mariposa Veterinary Wellness Center























